Article contents
Laboratory Alteration of Trioctahedral Micas
Published online by Cambridge University Press: 01 July 2024
Abstract
Artificial alteration of thirty-five trioctahedral and one dioctahedral micas by solutions varying in strength from 0·001 to 1·00 molal magnesium sulfate was found to approximate a normal exchange reaction after surface effects are eliminated. The equilibrium constants for the reaction:

range from 0·0001 to 0·0028 and average 0·0010 in value. X-ray diffraction study reveals that iron-rich micas tend to develop a 1:1 mixed-layer biotite-vermiculite structure in weak magnesium sulfate solutions whereas magnesium-rich biotite and phlogopite alter to vermiculite. Mica composition also influences the degree of alteration of mica to vermiculite. High fluorine and octahedral multivalent cation contents tend to retard the reaction whereas high magnesium content and perhaps high calcium contents tend to favor the alteration. The equilibrium constant data indicate that vermiculite and hydrobiotite are more stable than trioctahedral micas in most weathering environments.
Résumé
Trente cinq micas trioctaédriques et un mica dioctaédrique ont été altérés artificiellement par des solutions de sulfate de magnésium dont la concentration molale variait de 0,001 à 1,00. On a montré que l’altération pouvait se représenter par une réaction d’échange normale après élimination des effets de surface. Les constantes d’équilibre de la réaction
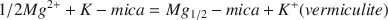
s’étagent de 0,0001 à 0,0028 avec une valeur moyenne de 0,0010. La diffraction des rayons X révèle que les micas riches en fer tendent à développer une structure interstratifiée 1:1 biotite-vermiculite dans les solutions de sulfate de magnésium peu concentrées tandis que les biotites riches en magnésium et les phlogopites s’altèrent en vermiculite. La composition du mica a aussi une influence sur le degré d’altération du mica en vermiculite. Les teneurs élevées en fluor et en cations octaédriques plurivalents tendent à retarder la réaction tandis que des teneurs élevées en magnésium et peut être en calcium tendent à la favoriser. Les valeurs des constantes d’équilibre indiquent que la vermiculite et l’hydrobiotite sont plus stables que les micas trioctaédriques dans la plupart des milieux d’altération naturelle.
Kurzreferat
Es wurde festgestellt, dass die künstliche Veränderung von fünfunddreissig trioktaed- rischen und einem dioktaedrischen Glimmer durch Lösungen, die in ihrem Gehalt von 0,001 bis 1,00 molar an Magnesiumsulfat variieren, sich einer normalen Austauschreaktion nähert, wenn man von den Oberflächeneffekten absieht. Die Gleichgewichtskonstanten für die Reaktion:
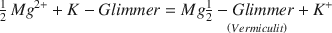
umfassen einen Bereich von 0,0001 bis 0,0028 mit einem Durchschnittswert von 0,0010. Untersuchungen mit Röntgenbeugung zeigen, dass eisenreiche Glimmer die Neigung haben ein 1:1 Mis- chschicht-Biotit-Vermiculit Gefüge in schwachen Magnesiumsulfatlösungen zu entwickeln’während magnesiumreicher Biotit und Phlogopit in Vermiculit verändert werden. Die Glimmerzusammensetzung beeinflusst auch den Grad der Veränderung von Glimmer in Vermiculit. Hohe Gehalte an Fluor und oktaedrischen vielwertigen Kationen neigen dazu die Reaktion zu verlangsamen, wohingegen hohe Magnesiumgehalte und vielleicht hohe Calciumgehalte die Veränderung eher begünstigen. Die Gleichgewichtskonstanten deuten darauf hin, dass Vermiculit und Hydrobiotit in den meisten Verwitterungsumgebungen stabiler sind als trioktaedrische Glimmer.
Резюме
Нашли, что исскуственное превращение тридцати пяти образцов триоктаэдральных и одного образца диоктаэдральной слюды растворами сернокислого магния различной крепости от 0,001 до 1,00 грамм-молекул приближенно выражает нормальную реакцию обмена после удаления поверхностных эффектов. Константы равновесия реакции следующие:
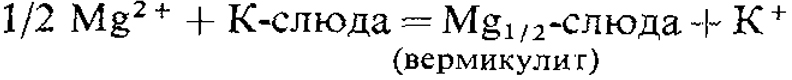
порядка от 0,0001 до 0,0028 и в среднем 0,0010. Рентгенографическими исследованиями обнаружили, что слюды богатые железом имеют тенденцию развивать в слабых растворах сернокислого магния смешанные пласты 1:1 структуры — биотита-вермикулита, в то время как биотит и флогопит богатые магнием превращаются в вермикулит. Высокое содержание фтора и октаэдрического многовалентного катиона замедляют реакцию, а высокое содержание магния и, может быть, кальция благоприятствуют превращению. Данные, константы равновесия указывают, что вермикулит и гидробиотит оказываются при выветривании более устойчивыми, чем триоктаэдральные слюды.
- Type
- Research Article
- Information
- Copyright
- Copyright © 1972, The Clay Minerals Society
References
- 25
- Cited by


